 |
DSNK_2000_7 zadaci
1. Navedene promjene tvari razvrstaj na fizikalne i kemijske:
A taljenje naftalena,
B zagrijavanje bakra na zraku,
C kondenzacija vodene pare,
D mjerenje temperature živinim termometrom,
E otapanje kisika u vodi,
F miješanje ulja i octa,
G reakcija bakrova(II) sulfata i vode,
H elektroliza vode,
I fotoliza srebrova bromida,
J djelovanje enzima katalaze na vodikov peroksid
a) Fizikalne promjene označene su slovima:_______________________________,
b) Kemijske promjene označene su slovima:_______________________________.
2. a) Koje navedene promjene prikazuju kemijsku sintezu, odnosno kemijsku analizu?
A sumpor(s) → sumpor(l),
B aluminij(s) + jod(s) → aluminijev jodid(s),
C kalijev klorid(s) → kalij(s) + klor(g),
D voda(l) → voda(g)
E amonijak(g) → dušik(g) + vodik(g),
F srebrov bromid(s) → srebro(s) + brom(l),
G natrij(s) + kisik(g) → natrijev oksid(s),
Kemijske sinteze označene su slovima:_______________________________,
Kemijske analize označene su slovima:_______________________________.
b) Kemijske promjene navedene po a) prikaži jednadžbama kemijskih reakcija.
c) Izračunaj masu joda koji je odreagirao s 25,0 g aluminija, ako je tom reakcijom dobiveno 377,5 g aluminijeva jodida.
3. Elektrolizom vode nastaju dva različita plina, a miješanjem tih plinova u istom volumnom omjeru u kojem nastaju dobiva se plin praskavac.
a) Navedi imena plinova koji čine sastav plina praskavca.
b) Izračunaj volumne udjele plinova u plinu praskavcu, ako je volumen jednog plina 50 mL, a volumen drugog plina 25 mL.
4. a) Shemom su prikazani najčešći načini dobivanja kisika.Napiši jednadžbe kemijskih reakcija za kemijske promjene označene u shemi brojevima od 1 do 4.
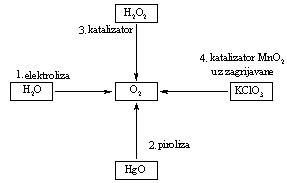
b) Koliko će molekula kisika nastati raspadom 6 molekula vodikova peroksida?
5. a) Kisik se industrijski može dobiti iz spoja A i smjese B.
Kemijski naziv spoja A je ______________ .
Naziv smjese B je ________________.
b) Nadopuni sljedeću rečenicu:
Smjesa B koja se koristi za dobivanje kisika mora biti u _______________ agregacijskom stanju, a postupak koji se pri tome koristi zove se _________________________.
6. Sumpornu kiselinu možemo proizvesti iz rude sfalerita. Napiši jednadžbe kemijskih reakcija koje su prikazane ponuđenom shemom.
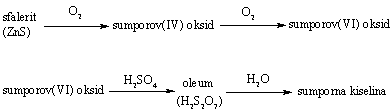
7. Reakcijom metala A (čuva se u petroleju i burno reagira s vodom) s otrovnim plinom B (žuto zelene boje) nastaje spoj C. Spoj C u reakciji sa sumpornom kiselinom daje bezbojan plin D (koji s vodenom parom iz zraka stvara bijelu maglu) i spoj E.
a) Prikaži gore navedene kemijske promjene jednadžbama kemijskih reakcija.
b) Imenuj tvari C, D, i E.
8. a) Dopuni opise kojima prikazujemo nastajanje nekih iona iz neutralnih atoma:
1. Ca(20p+ i 20 e-) → Ca2+(20p+ i _____ ) + ______________
2. Cl(17p+ i _____e-) + _____ → Cl-(_____p+ i _____e- )
3. Al(_____p+ i _____e-) → _____ (_____p+ i _____e- ) + _____e-
4. O(_____p+ i _____e-) + _____→ O2- (_____p+ i _____e- )
b) ione navedene u zadatku a) razvrstaj na katione i anione.
Kationi su: _____________________
Anioni su:______________________
c) Napiši jednadžbe kemijskih reakcija između tvari pod 1. i 2. i tvari pod 3. i 4. u zadatku pod a).
9. a) Pojmovima s lijeve strane pridruži brojeve ispred odgovarajućih pojmova s desne strane.

b) Prikaži reakcije tvari A, B, C s tvari D iz zadatka pod a).
c) Neki produkti iz zadatka pod b) reagiraju s vodom stvarajući hidrokside. Prikaži te kemijske promjene jednadžbama kemijskih reakcija.
10. U izvođenju pokusa pomiješali smo aluminij i sumpor. Maseni udio aluminija u toj smjesi iznosio je 35 %. Izračunaj:
a) maseni udio sumpora u danoj smjesi
b) masu aluminija i sumpora u 20 g smjese.
11. a) Razvojem industrije atmosfera Zemlje postaje sve zagađenija. Dio sumporovog(IV) oksida otapa se u kiši i pri tome nastane kiselina, a dio se oksidira uz prisutnost katalizatora. Reakcijom kiseline s kalcijevim karbonatom dolazi do oštećenja kamenih spomenika i građevina. Jednadžbama kemijskih reakcija prikaži gore navedene promjene.
b) Jedan od produkata u navedenim kemijskim promjenama pod
a) zamuti bistru vapnenu vodu. Prikaži i ovu kemijsku promjenu jednadžbom kemijske reakcije.
c) Tvari iz zadataka pod a) i b) razvrstaj na:
kiseline: __________________________________________,
okside:____________________________________________,
soli:_______________________________________________,
hidrokside:_________________________________________.
12. a) U nizu spojeva samo jedan spoj nije topljiv u vodi, a ako ga zapalimo gori.
SO3, P4O10, SO2, CO, MgO i CO2.
Napiši kemijski naziv toga spoja: _________________________________________.
b) Jednadžbom kemijske reakcije prikaži gorenje tog spoja.
c) Nadopuni sljedeću rečenicu.
Navedene spojeve ubrajamo u skupinu spojeva koje nazivamo
______________, a kemijsku reakciju _____________________.
13. Riješite li ispravno ispunjaljku dobit ćete, u uokvirenim poljima odozgo prema dolje, prezime osnivača moderne kemije. Napišite njegovo ime na crtu.
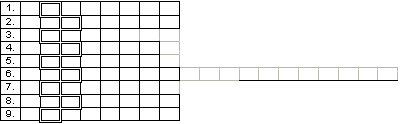
Vodoravno:
1. jednostavne tvari koje se ne mogu rastaviti na jednostavnije
2. kemijska promjena
3. materija (množ.)
4. složene čiste tvari
5. postupak spajanja dvije ili više tvari u jednu
6. spoj koji lakmusovu boju mijenja u crvenu
7. oznake elemenata
8. negativna čestica iz atoma
9. temperatura na kojoj tekućina ključa.
14. Plinovi X i Y su izgrađeni od dvoatomnih molekula. Molekule plina X sastoje se od atoma s protonskim brojem 1, a molekule plina Y od atoma s protonskim brojem 17.
a) Napiši nazive i kemijske znakove plinova X i Y.
Plin X je _________________ i označava se kemijskom formulom _________________.
Plin Y je _________________ i označava se kemijskom formulom _________________.
b) Reakcijom plinova X i Y nastaje kemijski spoj A. Napiši jednadžbu te kemijske reakcije.
c) Otapanjem spoja A u vodi nastaje spoj B, a njegov kemijski naziv je _____________________.
d) Spoj B u reakciji s čistom tvari protonskog broja 13 daje tvar C. Napiši jednadžbu te kemijske promjene.
15. Koje od navedenih jednadžbi kemijske reakcije su u skladu sa zakonom o održanju mase? Zaokruži slova ispred takvih jednadžbi.
A 2KMnO4 → K2MnO4 + MnO2 + O2,
B 2NO + O2 → NO2,
C Cu + HNO3 → Cu(NO3)2 + NO2 + 2H2O,
D 2ZnS + O2 → ZnO + SO2,
E P4O10 +H2O → H3PO4,
F 2Al(OH)3 → Al2O3 + 3H2O.
16. Mlijeko je smjesa različitih vrsta čistih tvari; masti, bjelančevina, mliječnog šećera i vode. Analizom mlijeka dobiveni su sljedeće podaci:
w(mast) = 3,6 %
w(bjelančevine) = 3,2 %
w(mliječni šećer) = 5,5 %
w(voda) = 87,7 %
Izračunaj masu vode koju sadrži 2 dL mlijeka, ako je gustoća mlijeka,
ρ(mlijeka) = 1,034 g cm-3.
|

